立足学情 创新发展——高三化学复习策略研究 |
一. 背景分析:
(一)2014年高考命题方向:
1. 2014年高考命题要坚持2013年命题方向,继续调整试卷结构,把握好学科间的平衡,确保在2013年的基础上稳定、持续、深化发展,使考试内容改革成效随时间显现更加充分。
2. 2013年北京市改革步伐加快,堪称“转折之年”,要研究高考试题,把握高考动向。
3. 准确把握学科教学现状和学生水平,处理好高考要求、课程实施要求及学生可接受度的关系,有效控制整卷难度,保证试卷内部的难度分布和梯度合理,实现良好的区分效果。
确定复习方向——抓住基础,狠抓落实,突出重点,突破难点。——策略一
(二)2014年命题原则:
命题采用学生熟悉的背景材料和语言,避免人为设置障碍和繁难偏怪,使学生能用熟悉的思维方式进行思考。关注学生接受基础教育期间所积累的基础知识,促进知识与技能、过程与方法、情感态度和价值观三维课程目标的实现。
理科综合要从学生已有的经验和将要经历的社会生活实际出发,以学生在日常生活和实验探究中所接触的科学事物和现象为基本内容,考查学生利用学科知识、学科思想和方法解决实际问题的能力;通过生产、生活中的一些真实情境和实验观察、自然体验,考查学生联系实际深化、应用知识的策略和学科素养。
明确考试的方向及培养学生的目标,有意识、有目的的应用在教学中。——策略二
(三)考查内容上的变化
1、知识上,重点和主干更加突出,更加关注基本原理的考查。更新的六道中有四道考查了基本原理,并对原理进行深度考查。
2、能力上,关注对接受、吸收、整合化学信息的能力的考查。具体表现在以下3个方面:第一,在更新的6道试题中,大部分均涉及到了对考生接受、吸收、整合化学信息的能力的考查。第二,信息给予形式的多样化,涉及文字、图(数据图、装置图)、表三类信息。第三,增加了对间接信息的接受、吸收、整合能力的考察。
3、方法上,关注对化学思想方法和思维品质的考查。在更新的6道试题的分析说明中,分别提及了对物质结构决定性质、分类与比较、物质的变化是有条件的、化学与社会和谐发展,宏观与微观、一般与特殊、定性与定量等思想方法上的考查。
总之,更新的试题更突出试题情境的“学科性”、“应用性”和“时代性”,更加注重考查化学本质的理解,更加注重对能力和思想方法的考查,更加注重综合性。
二. 我校学情:
1. 注重知识的衔接,同时注重学科知识的加深与拓展
我校使用的高三教材是《海淀区总复习指导》,它以高一、高二的知识为基础,作了合理的拓展与加深。从章节安排上分为四大部分:基本概念和基本理论、元素化合物知识、有机化学、化学实验,在知识体系上完整的体现基本概念和基本原理、元素化合物、化学计算、化学实验和化工基础几大板块。重视与会考与高考内容的合理衔接,注重科学态度和科学方法的培养,使学生逐步适应高考化学的要求。
2.学生学习在学习过程中的困难点调查结果
高三学生在学习化学的过程中遇到的困难,主要是知识难度及学习方法两方面,其中知识难度方面为35%,学习方法方面为16%,两者皆有占40%,合起来占81%高中化学难度明显增加,化学过程复杂,分析问题须从多方面多层次来探索研究,造成学生理解上的困难,抽象思维多于形象进行分析。在听课、完成作业、自学等方面仍停留在初中生的方法上,致使对高中化学的学习方法很不适应,造成了学习方法上的困难。
3. 注重学生综合素质的提高
素质教育的根本目的是教会学生学习,实现终身学习,终身受益。高三教材安排了丰富的阅读教材、选学内容、讨论题,这些内容的安排,促进教与学的形式多样化。阅读教材主要是要靠学生自学完成,它们无疑可以帮助学生提高自学能力,拓宽学生的知识面。选学内容则给教师更大的教学空间,教师可以根据教学内容、学生实际、生活中的化学问题、化工生产及高考的知识与能力要求,自主选择教学内容。按照讨论题给出的要求进行课堂讨论,是另外一种教学形式,学生在课堂上积极地与老师,与同学进行交流、对话、讨论,课后通过知识的加工整理,形成自已的知识网络并应用;同时,讨论题的安排还可以激发学生强烈的求知欲,培养学生发现问题、思考问题、解决问题的能力。
三、教学策略:
1、加强对学生学习策略、学法的指导,培养良好的学习习惯。
教师帮助学生掌握基本的学习方法,是一项重要的常规性工作。教师可以根据教学的各个环节,认真研究学生掌握基本学习方法的训练途径,比如:预习、听课、记笔记、做实验、做作业和复习小结(反思)等,针对每个环节的特点,加以指导,让学生形成良好的学习习惯,对学生良好学习习惯的养成,要持之以恒,要在“严”字上下功夫,真正做到落实,使学生终身受益。此外,针对化学学科的特点,对学生进行“学习策略”的教育和学法指导。比如,化学基本概念,基础知识,基本实验、基本计算等各类知识的学法指导,尤其应注意化学概念的形成及同化策略,化学知识与技能的迁移策略,化学问题解决的信息加工处理策略等。
2、加强实验、深化概念
安排一定数量的演示实验和学生实验,同时还有相当数量可利用实物、图片、模型,通过引导学生观察、思维,教会学生从大量感性认识中去加深对化学概念和原理的理解。加强直观性教学,不仅能给学生以启示,激发他们的兴趣,调动他们的学习积极性,而且还可以使概念和原理由抽象到具体,加深对概念的理解。学生往往对化学实验的现象感兴趣,忽视实验过程和实验设计与评价,导致实验能力差,高考时失分较多,教师应高度重视化学实验的规范培训和能力的培养。
3、抓住关键,精讲适练
教师在课堂教学中应充分发挥其主导作用,既不搞面面俱到,处处设防,讲得过细过全,也不能盲目让学生泛泛做题,以做代讲,而应抓住关键,讲其当讲,讲是讲清概念、原理、公式的来龙去脉,使学生透过表面现象,抓住其本质属性,弄清其内在联系。练其当练,练应有针对性,练是对概念、定律、物质性质的理解、巩固和应用,培养学生应用所学知识的能力。
案例:
《化学反应速率和化学平衡》一轮复习
【教学目标】
知识技能目标:
1、掌握图像的变化与化学反应条件改变之间的关系。
2、化学反应条件的改变对化学平衡移动的影响。
3、化学反应条件的改变对化学反应速率的影响。
过程方法目标:
1、通过学生对图像的分析,培养学生分析问题、解决问题的能力,提高学生的思维能力。
2、通过学生的总结归纳培养学生的综合概括能力,深入思维的能力。
情感态度价值观目标:
1、对图像的分析,培养学生对化学学科的兴趣及严密的思维逻辑性。
2、学生之间的合作交流精神。
【重点难点】
1、像中“点、趋势、量的变化”的关注力;
2、关注点”转化为判断“条件改变或平衡移动方向”的能力提升
【教学过程】
1. 由学生将早读习题按照图像、计算、等效平衡,将题型进行归纳整理
2. 以图像题为例,将1和5、2和8归为两类:一类转化率(或百分含量)-时间图、另一类某物质的浓度(或百分含量)-温度-压强图
【思考1】如何准确判断条件改变,平衡的移动方向,“关注点”是什么?
【思考2】在研究化学平衡移动方向及采取措施问题上“关注点”是什么?
【思考3】通过你的了解,你认为观察一个图像时,“关注点”有哪些?每个“关注点”变化有何规律?
【关注】学生课堂思维、知识表述、讨论情况和知识点的落实,突出解题方法和策略的引导,形成一类题目的完整思维过程。
【板书】
点:①如果只有一个点发生变化——此物质的浓度发生改变
②如果所有点均发生变化——改变了压强
③如果所有点均未发生变化,但平衡却发生改变——改变了温度
趋势: ①反应物减少,生成物增加——平衡正向移动
(平衡移动方向) ②反应物增加,生成物减少——平衡逆向移动
量:——变化量与系数成正比
(量的分析)
小结:
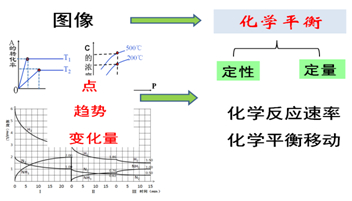
今天我们重点研究了用图像来认识和解决化学平衡问题,通过对这二类图像的研究,我们发现在观察图像时应重点观察“点、趋势和量的变化”,有利于我们对化学平衡进行定性和定量的分析。这节课我们主要研究了化学反应速率和平衡移动问题,后面我们还要从定量的角度继续对化学平衡研究。
【教学反思】
《化学反应速率和化学平衡》一轮复习的核心:复习巩固旧知识,寻找知识增长点。本节课针对图像问题,想达到:1. 通过对图像的分析,引发学生的“关注点”,形成观察图像的一般规律和方法。2. 通过学生对图像的分析,培养学生分析问题、解决问题的能力,提高学生的思维能力。3. 通过对所绘图像的分析总结,找到观察图像的方法,一般规律和解决办法。培养学生的总结概括能力,并以点带面,解决一类问题。
利用学案复习,突出了重点且进行知识点和命题点、命题方式的总结、概括,虽然前期备课量很大,需要把大量的题目进行精细的归纳、总结、整理,但总体呈现给学生的复习内容和知识点是完整的、清晰的,重点突出。
附:学生学案
化学反应速率与化学平衡
1. 在密闭容器中发生反应: ![]() ,其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图。下列判断正确的是:
,其中Z呈气态,且Z在平衡混合气中的体积分数(Z%)与温度(T)、压强(P)的关系如图。下列判断正确的是: 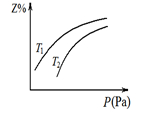
A.T1大于T2
B.Y一定呈气态
C.升高温度,该反应的化学平衡常数增大
D.当n(X):n(Y):n(Z)=1:3:2时,反应一定达到平衡状态
2. 一定条件下,向密闭容器中加入 X物质,发生反应 ![]()
反应一定时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示,下列说法中不正确的是:
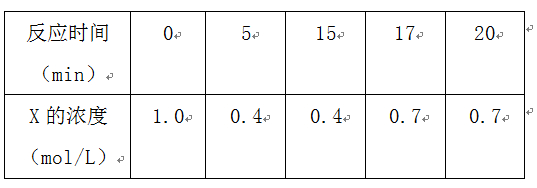
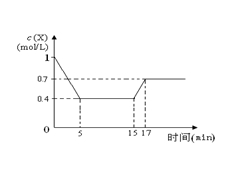
A.0~5 min时,该反应的速率为v(X)=0.12 mol/(L·min)
B.5 min时反应达到第一次平衡,该温度下的平衡常数数值为0.625
C.15 min时改变的条件不可能是升高温度
D.从初始到18 min时,X的转化率为30 %
3. PCl3和PCl5都是重要的化工原料。将PCl3(g) 和Cl2(g)充入体积不变的2 L密闭容器中,在一定条件下发生下述反应,并于10 min时达到平衡:
有关数据如下:
|
|
PCl3(g) |
Cl2(g) |
PCl5(g) |
|
初始浓度(mol/L) |
2.0 |
1.0 |
0 |
|
平衡浓度(mol/L) |
c1 |
c2 |
0.4 |
下列判断不正确的是:
A.10 min内,v(Cl2) = 0.04 mol/(L·min)
B.当容器中Cl2为1.2 mol时,反应达到平衡 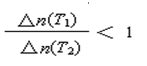
C.升高温度(T1<T2),反应的平衡常数减小,平衡时PCl3的
D.平衡后移走2.0 mol PCl3和1.0 molCl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol/L
4.一定条件下,分别向容积固定的密闭容器中充入A和足量B,发生反应如下:
![]() 测得相关数据如下,分析可知下列说法不正确的是:
测得相关数据如下,分析可知下列说法不正确的是:
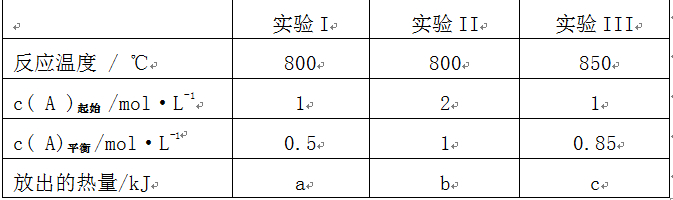
A.实验III的化学平衡常数K<1
B.实验放出的热量关系为b>2a
C.实验III 在30min达到平衡时的速率v (A)为0.005mol·L-1·min-1
D.当容器内气体密度不随时间而变化时上述反应已达平衡
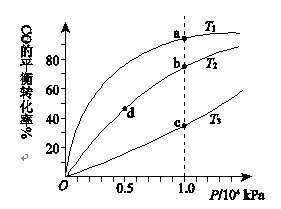
5.用CO合成甲醇(CH3OH)的化学方程式为 ![]() ,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示。
,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右下图所示。
下列说法不正确的是:
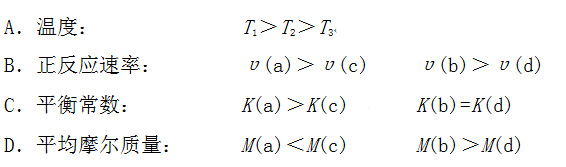
6.下列图示与对应的叙述相符的是:
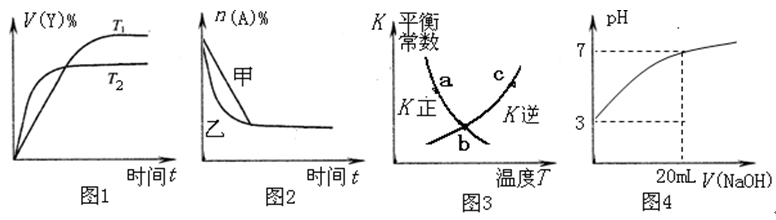
A.图1表示可逆反应
B.图2表示压强对可逆反应
C.图3中a、b、c三点中只有b点已经达到化学平衡状态
D.图4是向20 mL pH = 3 的醋酸溶液中滴加 pH=11的NaOH溶液过程中pH变化曲线
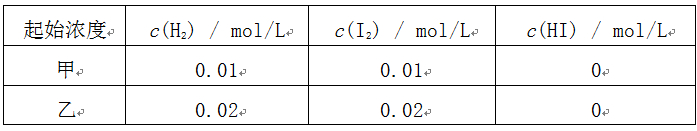
7.已知: ![]()
某温度下在甲、乙两个恒容密闭容器中充入反应物,其起始浓度如下表所示。甲中反应达到平衡时,测得c(H2)=0.008 mol/L。 下列判断正确的是:
A.平衡时,乙中H2的转化率是甲中的2倍
B.平衡时,甲中混合物的颜色比乙中深
C.平衡时,甲、乙中热量的变化值相等
D.该温度下,反应的平衡常数K=0.25
8.反应 ![]() 在等容条件下进行。改变其它反应条件,
在等容条件下进行。改变其它反应条件,
在I、II、III阶段体系中各物质浓度随时间变化的曲线如下图所示,下列说法不正确的是:
A.反应的化学方程式中,a : b : c=1 : 3 : 2
B.A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A),最大的是vⅠ
(A)
C.第II阶段反应温度小于第III阶段反应温度
D.由第一次平衡到第二次平衡,采取的措施是从反应体系中移走C